Sacituzumab govitecan è un antibody-drug conjugate (ADC) diretto contro l’antigene di superficie trofoblastico (Trop-2), coniugato con il metabolita attivo dell'irinotecan (SN-38). È già approvato per il trattamento delle pazienti con carcinoma della mammella triplo negativo pretrattate. In questo trial di fase III TROPiCS-02, sono state randomizzate 543 pazienti con carcinoma della mammella metastatico HR+/HER2-, ormono-resistenti, pretrattate, a ricevere sacituzumab govitecan (10 mg/kg ev g 1,8 q21) oppure chemioterapia a scelta dello sperimentatore (eribulina, vinorelbina, capecitabina o gemcitabina). Endpoint primario: progression-free survival (PFS).
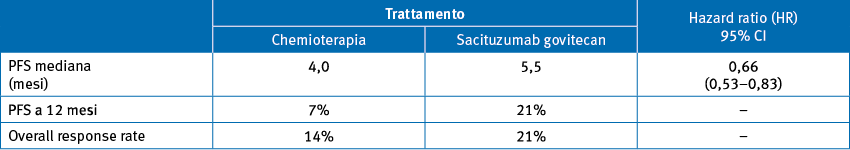
Il 99% delle pazienti aveva ricevuto un precedente trattamento con un inibitore della chinasi ciclina-dipendente 4/6 (CDK4/6i) e con tre linee mediane di chemioterapia per la malattia avanzata. I dati di overall survival (OS) non sono ancora maturi. Gli eventi avversi di grado 3-4 correlati al trattamento più frequenti sono stati neutropenia (51% nel braccio sperimentale vs 38% nel braccio della chemioterapia standard), leucopenia (9 vs 5%), diarrea (9 vs 1%), anemia (6 vs 3%) e fatigue (6 vs 2%).